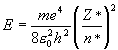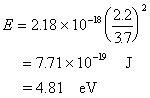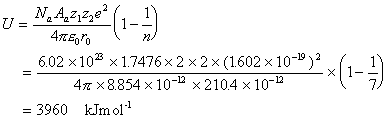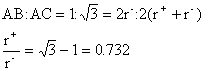–³‹@‰»ٹwٹî‘b |
||||||||||||
| –³‹@‰»ٹw‡T‰‰ڈK–â‘è‰ً“ڑ 1.
پi—zژqپ{“dژqپj8Œآپ{’†گ«ژq8Œآ = 1.007825پ~8 + 1.008665پ~8 = 16.13192 mu ژہچغ‚جژ؟—تپ@15.994915 mu چ·•ھپ@0.137005 mu
K 1s22s22p63s23p64s1 Z*=19-(0.85پ~8+1پ~10)=2.2 n*=3.7
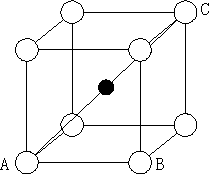
sp2چ¬گ¬‚ة‚و‚ء‚ؤ•½–ت“à‚إ3•ûŒü‚ة‹O“¹‚ھ‚إ‚«پA‚»‚ꂼ‚ê‚ج‹O“¹‚إŒ‹چ‡“dژq‘خ‚ًŒ`گ¬‚µ‚ؤ‚¢‚éپB‚»‚ج‚½‚كB‚ً’†گS‚ئ‚·‚镽–تژOٹpŒ`‚ئ‚ب‚éپB NH3پ@Nپ@1s22s22p3پ¨1s2(2s2px2py2pz)5پ@sp3چ¬گ¬ sp3چ¬گ¬‚ة‚و‚ء‚ؤN‚ً’†گS‚ئ‚·‚éژl–ت‘ج‚ج’¸“_•ûŒü‚ة‚S‚آ‚ج‹O“¹‚ھ‚إ‚«‚éپB‚±‚ê‚ç‚ج‹O“¹‚ة‚حN‚©‚ç‚TŒآ‚ج“dژq‚ھ‚ح‚¢‚邽‚كپAˆê‚آ‚ج”ٌ‹¤—L“dژq‘خ‚ئ‚R‚آ‚جŒ‹چ‡“dژq‘خ‚ًŒ`گ¬‚·‚éپBŒ‹‰ت‚ئ‚µ‚ؤNH3‚حN‚ً’¸“_‚ئ‚·‚éژOٹpگچ‚جŒ`‚ئ‚ب‚éپB‚ـ‚½پA“dژq‘خ”½”‘¥‚ة‚و‚èپAپعH-N-H‚حگ³ژl–ت‘ج‚جڈêچ‡پi109پ‹28پfپj‚و‚è‚àڈ¬‚³‚ب’l‚ئ‚ب‚éپB
(b)ژO•û—¼گچپ@dsp3 (c)گ³”ھ–ت‘جپ@d2sp3 (d)پiکc‚ٌ‚¾پjژOٹpگچپ@sp3پ@NH3‚ئ“¯‚¶پB
8.
9.پ@ƒ{ƒ‹ƒ“پ|ƒnپ[ƒoپ[ƒTƒCƒNƒ‹ RbF(Œإ) پ© Rb+(‹C)پ{F-(‹C)
Rb(Œإ)پ{1/2F2(‹C) پ¨ Rb(‹C)پ{F(‹C)
-552=78+402+80+x-762 x=-350 kJmmol-1 “dژqگeکa—حپ@350 kJmol-1
11. Rb+پABr-‚حKr‚ج“dژq”z’u‚ً‚à‚آپB Kr=1s22s22p63s23p63d104s24p6 s=0.35پ~8+0.85پ~18+1پ~10=28.1 Z*(Rb+)=37-28.1=8.9, Z*(Br-)=35-28.1=6.9 r(Rb+)=342پ~6.9/(8.9+6.9)=149pm r(Br-)=193pm 12.
(a)ٹ·ژZژ؟—ت
=1:1.000365 0.0365% (b)13.6پ~0.000365=4.96پ~10-3eV‘ه‚«‚¢ 13.پ@(a)پ@‡B‚و‚è
(b)پ@‡A‚ئ‡H‚و‚è
‚µ‚½‚ھ‚ء‚ؤپA
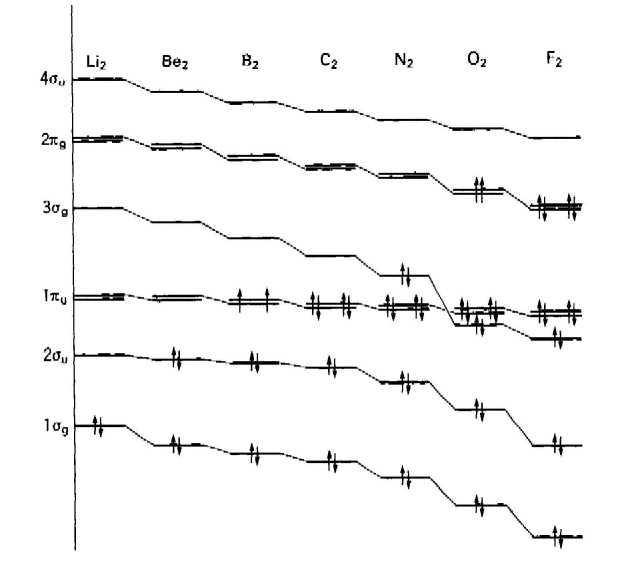
14. (a)ƒCƒIƒ“‰»ƒGƒlƒ‹ƒMپ[‚حپA‘S‘ج‚ئ‚µ‚ؤ‘‰ء‚·‚é‚ھپAAl‚¨‚و‚رS‚ج‚ئ‚±‚ë‚ة‚ض‚±‚ف‚ھ‚ ‚éپB (b)“dژqگeکa—ح‚ح‘‰ء‚·‚éŒXŒü‚ًژ¦‚·‚ھپAMgپAPپAAr‚ح—لٹO‚إ‚ ‚éپB (cپj“d‹C‰Aگ«“x‚ح’Pڈƒ‚ة‘‰ء‚·‚éŒXŒü‚ًژ¦‚·پB 15. 02:(1ƒذg)2(2ƒذu)2(3ƒذg)2(1ƒخu)4(2ƒخg)2
16.
17. C‚©‚çN‚ضچs‚‚ئ‚«گV‚½‚ة‰ء‚ي‚é“dژq‚ح‹َ‚ج2p‹O“¹‚ة“ü‚é.N‚©‚çO‚ضچs‚‚ئ‚«‚ة‚ح,‚آ‚¬‚ج“dژq‚ھ“ü‚é2p‹O“¹‚ھ‚·‚إ‚ة1Œآ‚ج“dژq‚إگè‚ك‚ç‚ê‚ؤ‚¢‚é.‚µ‚½‚ھ‚ء‚ؤ,‚±‚ج‚ئ‚«‚ة‰ء‚ي‚ء‚½“dژq‚ح‚و‚è‹‚¢”½”‚ًژَ‚¯‚é‚ج‚إ,ٹj‚ج“d‰×‚ج‘‰ء•ھ‚ھ‘إڈء‚³‚ê‚é’ِ“x‚حC‚©‚çN‚ض‚جڈêچ‡‚و‚è‚à’ک‚µ‚‚ب‚é. |